Эпидемиология сахарного диабета в Российской Федерации: что изменилось за последнее десятилетие?


Опубликована Окт. 1, 2019
Последнее обновление статьи Ноя. 22, 2022
Аннотация
Резюме
В результате работы регистра сахарного диабеты (СД) создана единая динамическая база данных в онлайн-формате, что позволяет осуществлять клинико-эпидемиологический мониторинг СД в масштабах всей страны.
Цель исследования. Провести анализ эпидемиологических характеристик СД за последнее десятилетие, отразить динамику распространенности острых (комы) и хронических (микро- и макрососудистых) осложнений СД.
Материалы и методы. Объектом исследования являлась деперсонифицированная база данных регистра СД - 84 региона РФ, включенных в систему онлайн-регистра на 01.01.2019 г.
Результаты и обсуждение. Общая численность пациентов с СД в РФ на 01.01.2019 г. составила 4 584 575 (3,12% населения РФ), в том числе: СД1 - 256,2 тыс., СД2 - 4,24 млн, другие типы СД - 89,9 тыс. С 2000 г. численность пациентов с СД в РФ выросла в 2,2 раза. Количество пациентов в 2018 г. с целевым уровнем НЬА1с <7% при СД1 - 34,7%, при СД2 - 52,2%. При сравнении с данными 2007 г. отмечается снижение осложнений при СД1/СД2: кетоацидотических ком в 3/4 раза, слепоты в 2/4,4, синдрома диабетической стопы в 1,5/3 раза, соответственно. После перевода регистра в онлайн-формат стал доступен более подробный анализ осложнений СД в динамике 2013-2017 гг. В статье представлены данные о распространенности диабетической ретинопатии и слепоты, хронической болезни почек, синдрома диабетической стопы, ампутаций и сердечно-сосудистых осложнений при СД.
Заключение. Несмотря на продолжающееся увеличение численности пациентов с СД, за последнее десятилетие в РФ достигнуто значимое снижение распространенности осложнений, улучшилось качество их диагностики. Приоритетным направлением повышения качества диабетологической помощи является развитие специализированной помощи при СД на всех уровнях от первичного звена до лечебных учреждений третьего уровня и региональных центров диабета в субъектах РФ, а также стандартизация алгоритмов обследования и методов ранней диагностики.
Ключевые слова
Диабетическая нефропатия, сердечнососудистые осложнения, распространенность сахарного диабета, синдром диабетической стопы, ампутация, сахарный диабет, хроническая болезнь почек, диабетическая ретинопатия, кома, регистр сахарного диабета
АУ — альбуминурия
ГРСД - Государственный регистр сахарного диабета
ДН - диабетическая нефропатия
ДР — диабетическая ретинопатия
ЗПА - заболевания периферических артерий
ИБС — ишемическая болезнь сердца
ИМ - инфаркт миокарда
СД - сахарный диабет
СД1 - сахарный диабет 1-го типа
СД2 - сахарный диабет 2-го типа
СДС — синдром диабетической стопы СКФ — скорость клубочковой фильтрации
ССЗ - сердечно-сосудистые заболевания
ССТ - сахароснижающая терапия ФЦП - Федеральная целевая программа ХБП — хроническая болезнь почек
ЦВЗ - цереброваскулярные заболевания НЬАІс — гликированный гемоглобин IDF - Международная федерация диабета
Введение
Снижение медико-социального ущерба, обусловленного глобальным ростом распространенности сахарного диабета (СД) и его осложнений, является одной из наиболее приоритетных задач национальных систем здравоохранения во всем мире.
С этой целью в Российской Федерации (РФ) разработана Федеральная целевая программа (ФЦП) «Сахарный диабет». Одним из ключевых направлений реализации ФЦП стало создание системы клинико-эпидемиологического мониторинга СД в масштабах всей страны посредством Государственного регистра сахарного диабета (ГРСД). ГРСД основан Приказом Минздрава России от 10.12.1996 г. №404; методологическим и организационным референс-центром регистра стал ФГБУ «Эндокринологический научный центр» (ныне «НМИЦ эндокринологии» Минздрава России) [1].
Более чем за 20-летний период работа регистра сыграла ключевую роль в оценке распространенности СД и диабетических осложнений в РФ. С 2014 г. регистр трансформирован в единую федеральную базу данных с авторизированным кодом доступа, работающую в онлайн-формате, что позволило повысить ее эффективность в качестве ключевой информационно-аналитической платформы [2].
В настоящей работе представлен динамический анализ эпидемиологических характеристик СД за последнее десятилетие, наиболее важных с позиций вектора развития диабетологической помощи в РФ и оценки ее качества; отражена динамика распространенности острых (комы) и хронических (микро- и макрососудистых) осложнений СД в динамике в период 2013-2017 гг. по сравнению с периодом реализации ФЦП «Сахарный диабет» 2007-2012 гг.
Методология анализа эпидемиологических показателей.
Объектом исследования являлась деперсонифицированная база данных регистра СД - 84 региона РФ, включенных в систему онлайн-регистра на 01.01.2019 г.
Распространенность СД рассчитывалась на 100 тыс. населения соответствующих возрастных групп: дети в возрасте <15 лет, подростки в возрасте от 15 до 18 лет, взрослые - лица старше 18 лет (>18 лет); распространенность осложнений представлена у взрослых пациентов с СД 1-го и 2-го типа (СД1 и СД2) на 10 тыс. пациентов с СД соответствующего типа. Данные динамики осложнений представлены в процентном отношении по сравнению с опубликованными данными ФЦП 2007-2012 гг. [3].
Распространенность — показатель, оценивающий количество всех зарегистрированных случаев заболевания (осложнения).
Заболеваемость (первичная, по обращаемости) - показатель, оценивающий количество новых случаев заболевания (осложнения), впервые зарегистрированных в текущем календарном году.
Регистрация осложнений в регистре осуществляется согласно современной классификации, представленной в «Алгоритмах специализированной медицинской помощи» [4].
К острым осложнениям СД относят диабетический кетоацидоз, гиперосмолярное гипергликемическое состояние, лактатацидоз и гипогликемию. В случае потери сознания данные состояния фиксируются как комы соответствующего генеза.
К диабетическим микроангиопатиям относят ретинопатию и нефропатию. В регистре фиксируется уровень альбуминурии, проводится автоматический расчет скорости клубочковой фильтрации (СКФ) по формуле CKD-EPI, что позволяет установить диагноз хронической болезни почек (ХБП) в соответствии с современными стандартами диагностики в автоматическом режиме. Развитие слепоты регистрируется при полной потере зрения (visus - 0) на одном или обоих глазах.
К макрососудистым осложнениям принято относить ишемическую болезнь сердца (ИБС), цереброваскулярные заболевания (ЦВЗ) и заболевания периферических артерий (ЗПА). Инфаркт миокарда (ИМ) является одной из клинических форм ИБС. В настоящей статье представлен анализ отдельных нозологий: ИБС, ИМ и острых форм ЦВЗ (острые нарушения мозгового кровообращения и транзиторные ишемические атаки).
Наличие синдрома диабетической стопы (СДС) согласно современной классификации регистрируется при наличии язвы нижних конечностей и/или остеоартропатии (стопы Шарко) и его терминального исхода - ампутаций нижних конечностей.
Распространенность сахарного диабета в РФ
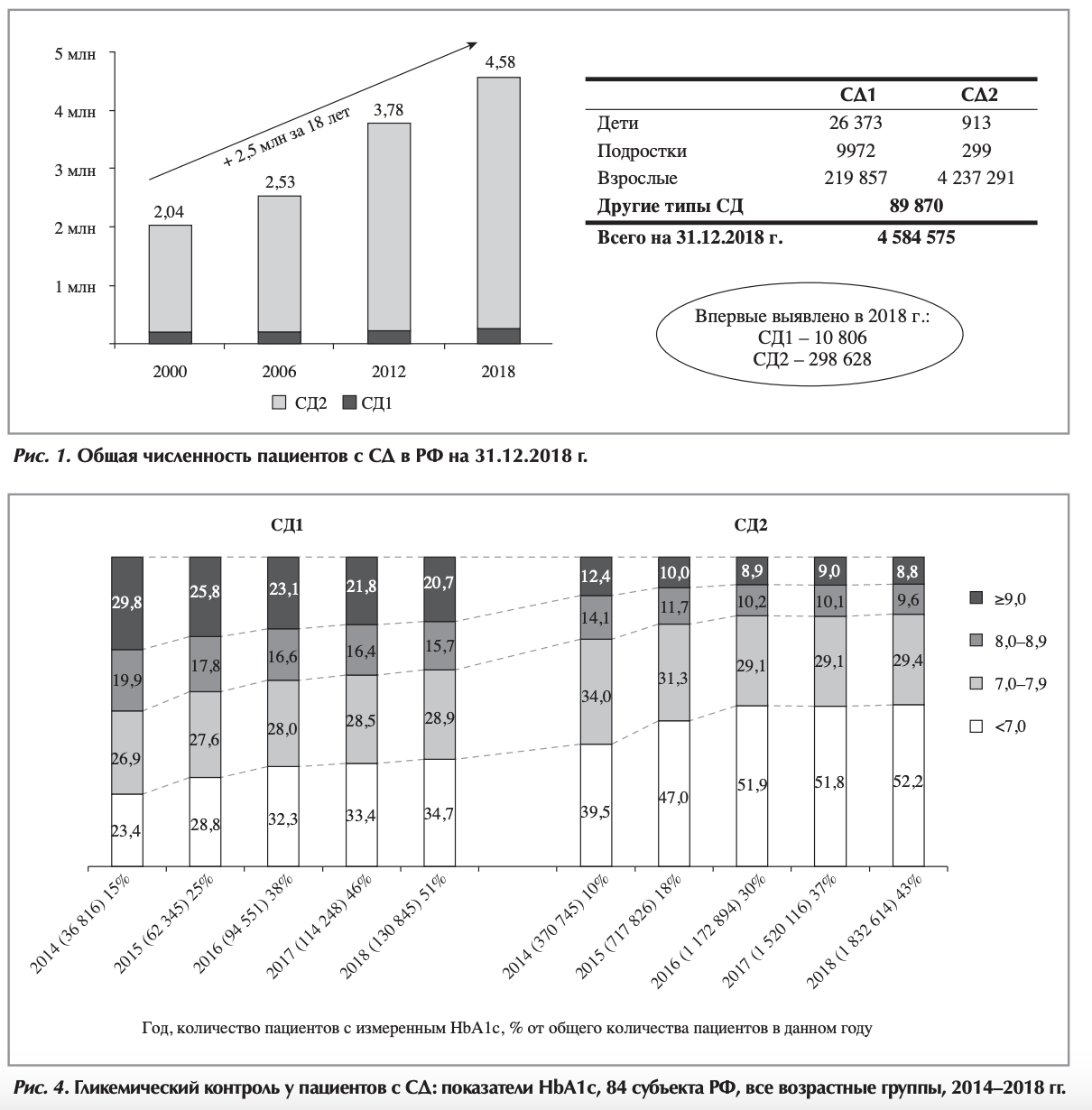
Общая численность пациентов с СД в РФ на 01.01.2019 г. составила 4 584 575 (3,12% населения РФ), в том числе: СД1 - 5,6% (256,2 тыс.), СД2 - 92,4% (4,24 млн), другие типы СД - 2% (89,9 тыс.; рис. 1).
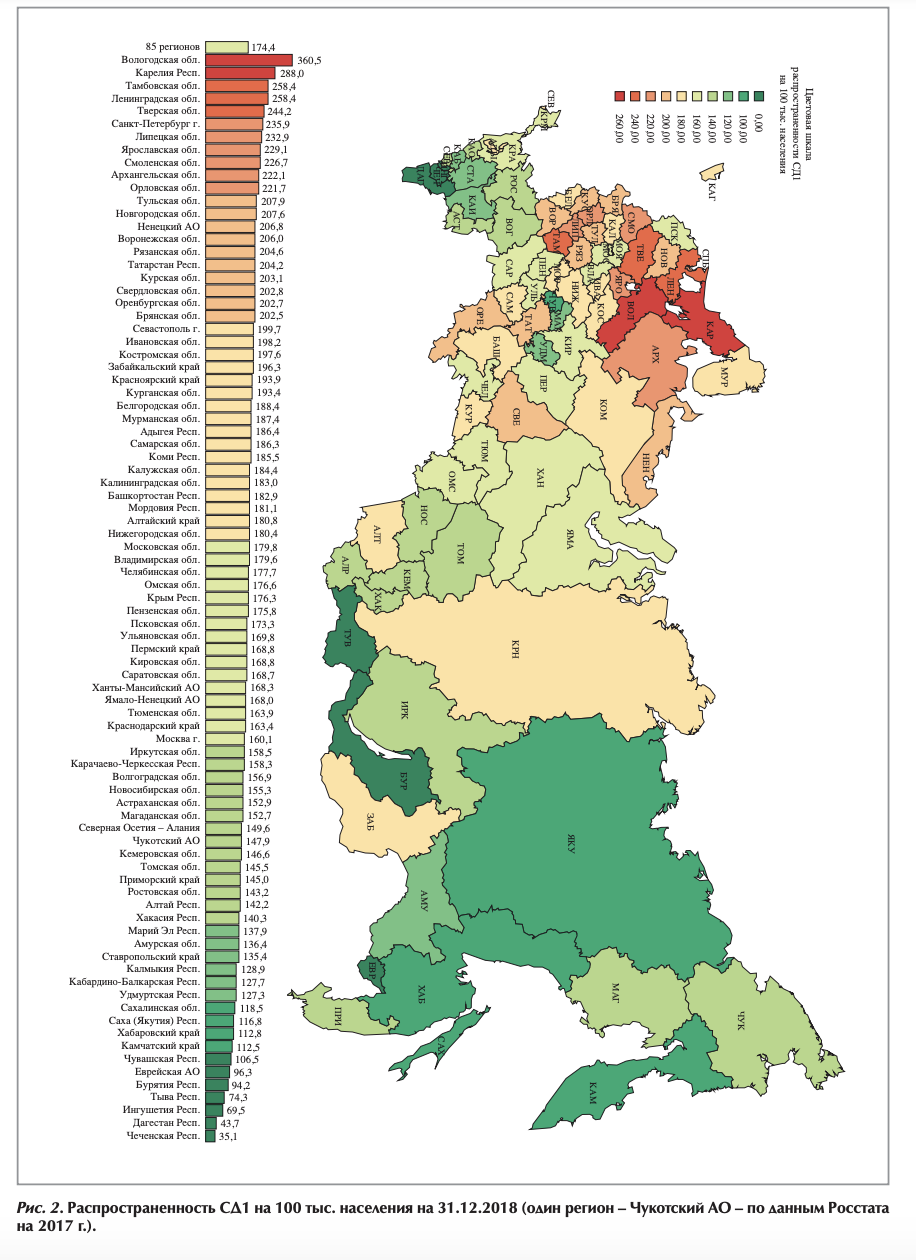
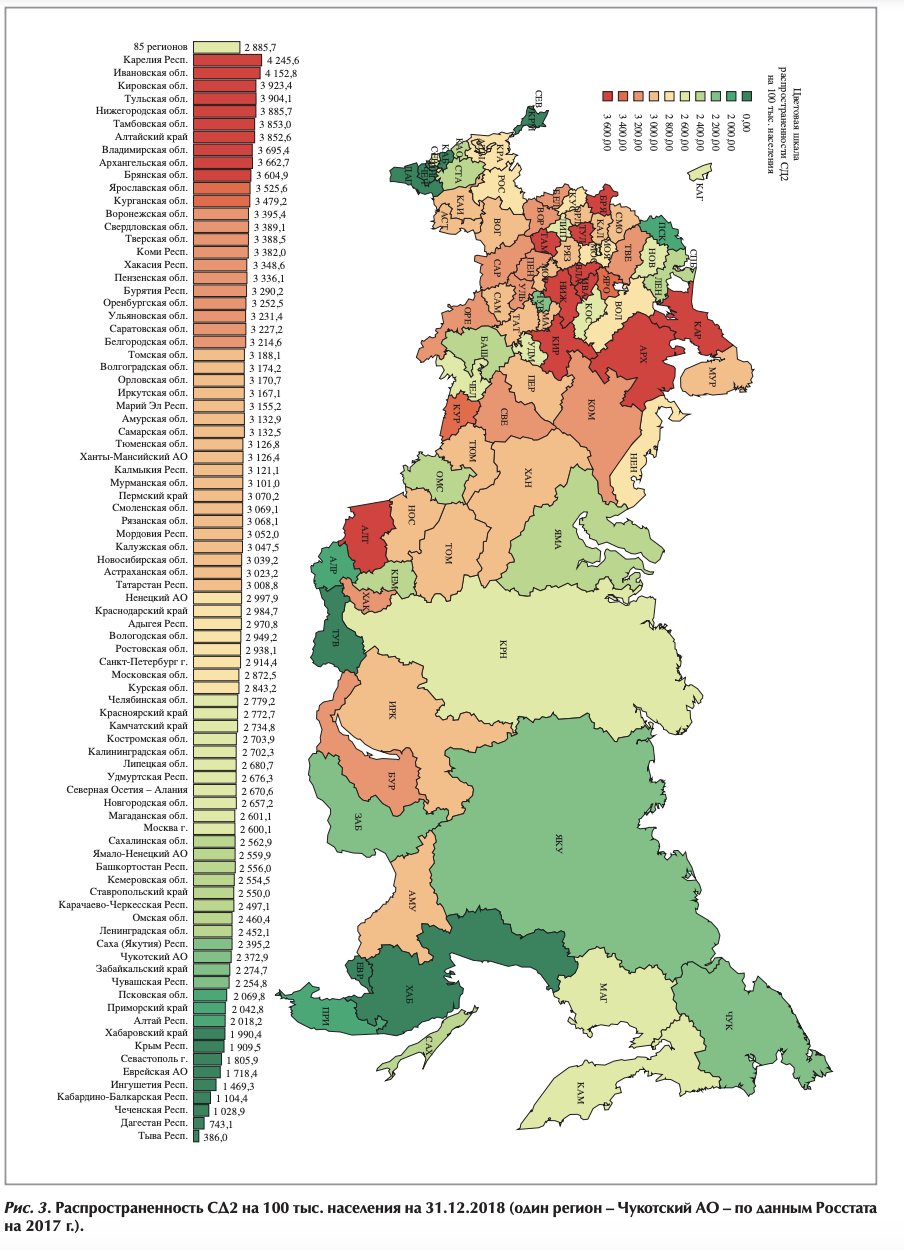
В настоящее время средняя распространенность СД1 составляет 174,4 на 100 тыс. населения, СД2 - 2885,7 на 100 тыс., других типов СД - 61,2 на 100 тыс. населения, выделяются регионы с более высокими показателями. Данные распространенности СД1 и СД2 в 85 субъектах РФ на 01.01.2019 г. представлены на рис. 2 и 3 (см. на цветной вклейке), соответственно; Чукотский автономный округ (не включенный в онлайн-регистр) представлен по данным Федеральной службы государственной статистики (Росстат) [5].
С 2000 г. численность пациентов с СД в РФ выросла в 2,2 раза - с 2,043 млн [2] до 4,58 млн человек. Как и во многих странах мира [6, 7], в РФ продолжается рост распространенности СД, преимущественно СД2, с ежегодным увеличением не менее чем на 250-300 тыс. пациентов. В течение 2018 г. выявлено 10 805 новых случаев СД1 и 298 628 - СД2.
Однако и эти цифры недооценивают истинные масштабы неинфекционной «эпидемии». Дело в том, что в регистре фиксируются только выявленные случаи заболевания. Так, по данным национального эпидемиологического исследования NATION, включившего более 26 тыс. человек в 63 субъектах РФ, доля не выявленного СД2 в РФ в среднем составляет 54% [8]. Таким образом, фактическая распространенность СД2 при активном скрининге по уровню гликированного гемоглобина (НЬАІс) почти в 2 раза выше регистрируемой и может достигать 8-9 млн человек [8]. Эти данные еще раз подчеркивают необходимость государственных мер, направленных на разработку программ активного выявления СД в группах риска.
Анализ состояния компенсации углеводного обмена
Среди методов, с позиций доказательной медицины продемонстрировавших наиболее высокую эффективность в снижении риска диабетических осложнений, достижение целевого контроля гликемии является наиболее значимым.
Именно с этих позиций оценка уровня HbA1c является не только важнейшим лабораторным показателем, определяющим стратегию в отношении интенсификации терапии, но и ключевым целевым индикатором качества оказания диабетологической помощи в целом.
За последние годы мы действительно можем констатировать существенную положительную динамику гликемического контроля: увеличение количества пациентов с целевым уровнем HbA1c <7% и снижение доли декомпенсированных пациентов с уровнем HbA1c >9,0% (рис. 4). И тем не менее
приходится признать, что данный показатель оценивается (или вносится в Регистр) только у 44% пациентов (у 51% с СД1 и 43% с СД2). Таким образом, значительная доля пациентов с СД остается вне зоны контроля эффективности сахароснижающей терапии, а соответственно, и прогноза в отношении риска развития осложнений. Это факт требует консолидации усилий органов здравоохранения и всех медицинских специалистов, работающих с пациентами с СД, направленных на повышение доступности исследования НЬАІс вне зависимости от места жительства пациента и увеличение кратности измерения данного параметра - в соответствии со стандартами оказания специализированной диабетологической помощи [4].
Анализ динамики диабетических осложнений
Первые результаты по снижению частоты диабетических осложнений получены в период реализации подпрограммы ФЦП «Сахарный диабет» (2007-2012) [3] благодаря масштабным государственным мерам, направленным на развитие диабетологической службы в РФ, созданию специализированных кабинетов диабетической ретинопатии (ДР) и диабетической стопы, «Школ для пациентов с СД» и внедрению структурированных программ обучения, развитию системы подготовки медицинских специалистов. Анализируя динамику распространенности осложнений в последние годы, мы можем констатировать сохранение этих положительных тенденций. В целом за прошедший 10-летний период достигнуто снижение частоты различных диабетических осложнений (рис. 5, см. на цветной вклейке).
Особое значение приобретает снижение частоты острых осложнений, ассоциированных с высоким риском смертности, - кетоацидотических ком: в 3 раза при СД1 (с 3,3 до 1,25%) и в 4 раза при СД2 (с 0,2 до 0,05%), а также тяжелых хронических осложнений, ведущих к инвалидизации, таких как слепота - в 2 раза при СД1 (с 2,0 до 0,99%) и в 4,4 раза при СД2 (с 0,71 до 0,16%) и СДС -в 1,5 раза при СД1 (с 6,3 до 4,3%) ив 3 раза при СД2 (с 5,1 до 1,7%).
В настоящее время, после перевода регистра в онлайн- формат, стал доступен более подробный анализ осложнений СД, мы можем более детально изучать динамику заболеваемости, распределение по стадиям, распространенность различных форм, длительность СД и возраст на момент развития осложнений.
Диабетические комы
При оценке динамики развития ком в период 2013-2017 гг. отмечается снижение распространенности ком при обоих типах СД, что продолжает тенденции предыдущего периода ФЦП 2007-2012 гг. Частота новых случаев ком в год в РФ в среднем сократилась более чем в 2 раза: с 0,9 до 0,4 на 10 тыс. взрослых пациентов с СД; при оценке по типам СД - при СД1 с 5,7 до 3,4 на 10 тыс. взрослых пациентов, при СД2 с 0,6 до 0,2 на 10 тыс. взрослых пациентов [9].
С достаточной долей уверенности можно говорить, что это связано с улучшением качества оказания диабетологической помощи и гликемического контроля в целом, а также использованием современных лекарственных препаратов.
В последние годы благодаря внедрению в клиническую практику новых подходов к сахароснижающей терапии (ССТ), повышению доступности современных сахароснижающих препаратов, в том числе аналогов инсулинов, которые лучше имитируют физиологический ритм секреции, эпидемиологическая ситуация по частоте ком значительно улучшилась, о чем свидетельствуют как отечественные, так и мировые данные [2, 3,10-12]. Развитие «Школ диабета» и внедрение структурированных программ обучения пациентов с СД остаются ведущим фактором профилактики ком.
При оценке структуры различных видов ком выявлено перераспределение за счет сокращения кетоацидотических ком при увеличении доли ком, имеющих гипогликемический генез, особенно выраженное при СД1 [9].
Это имеет важнейшее значение, поскольку последнее десятилетие отмечено повышением интенсивности ССТ и снижением целевых значений гликемического контроля при СД, обоснованном результатами крупномасштабных контролируемых исследований. Аналогичные тенденции увеличения частоты гипогликемий, требующих госпитализации, продемонстрированы при анализе базы данных Англии в периоды с 1998 по 2009 г. и с 2009 по 2013 г., т. е. в периоды с различными подходами к интенсификации ССТ в рутинной клинической практике. Авторы выявили, что у пациентов в возрасте до 65 лет ежегодный прирост частоты госпитализаций вследствие гипогликемий составил 4,12% (0,61-7,75%), а в группе пациентов старше 65 лет он в 2 раза выше - 8,12% случаев [13].
Эти данные еще раз подчеркивают необходимость персонализированного подхода при оптимизации контроля СД, в том числе к установлению целевого уровня НЬАІс для каждого конкретного пациента с учетом всех возможных рисков и коморбидных состояний, с целью снижения развития тяжелых гипогликемий и ком гипогликемического генеза.
Диабетическая ретинопатия
ДР - наиболее частое поражение глаз при СД, ведущее к значительному снижению остроты зрения вплоть до полной его потери, что определяет клиническую и социальную значимость изучения данной патологии.
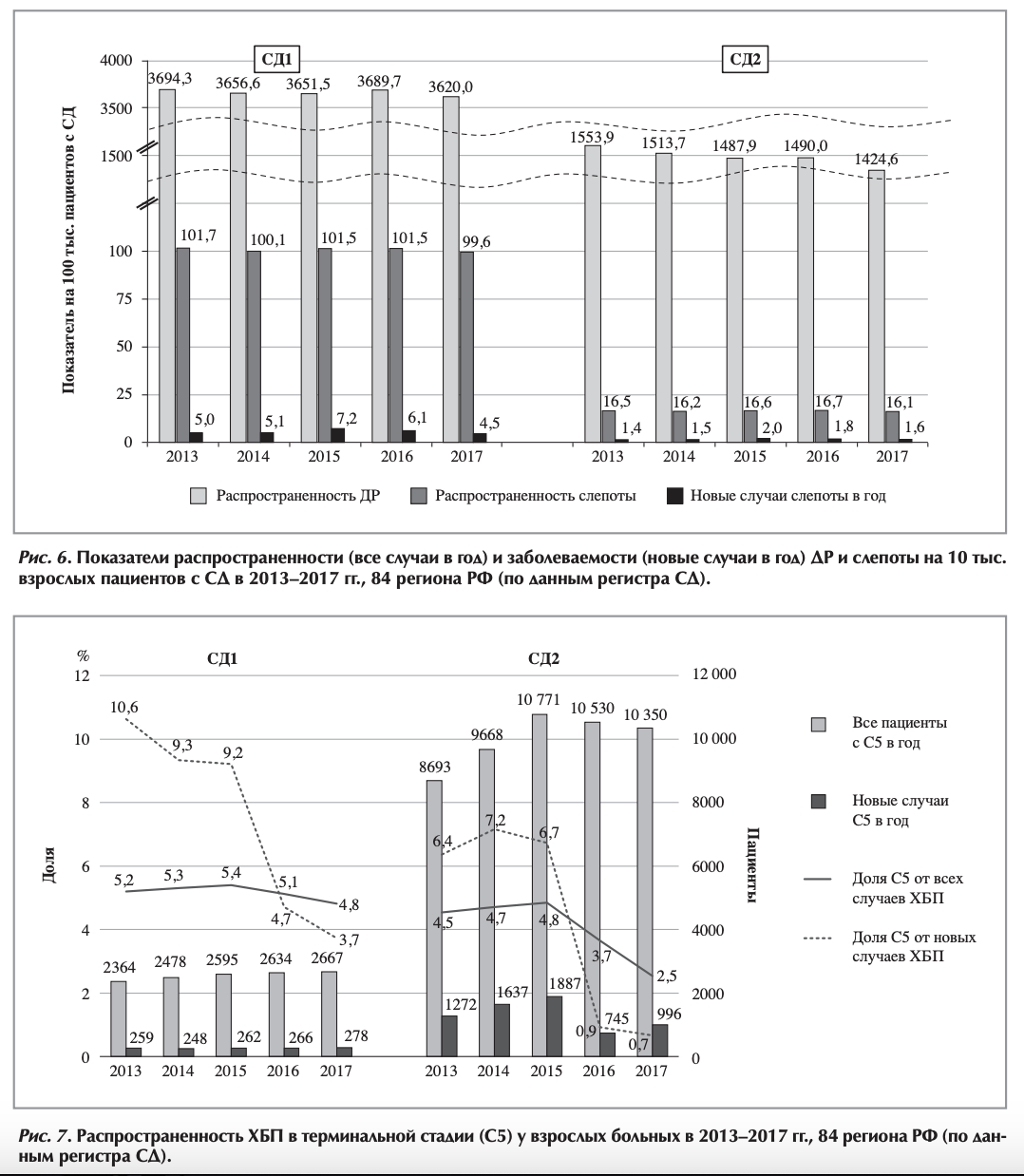
В РФ за прошедшее десятилетие отмечается снижение частоты ДР при обоих типах СД (с 42,6 до 36,2% при СД1 и с 24,7 до 14,2% при СД2; рис. 6, см. рис. 5 на цветной вклейке). И особенно значимые результаты достигнуты по снижению риска развития слепоты - в 2 раза при СД1 и в 4,4 раза при СД2 (см. рис. 5 на цветной вклейке), что имеет приоритетное значение для повышения качества жизни этих пациентов.
Анализ данных регистра указывает на значимое улучшение качества диагностики ДР: в настоящее время осложнение диагностируется у 70,4% пациентов с СД1 и у 81% при СД2 на начальной (непролиферативной) стадии [14]. При этом следует подчеркнуть значительные межрегиональные различия в частоте ДР, варьирующей от 2,6 до 66,1% при СД1 и от 1,1 до 46,4% при СД2 [14]. Столь выраженные межрегиональные различия могут быть связаны с отсутствием соблюдения единых стандартов диагностики ДР (исследование сетчатки с широким зрачком, кратность осмотра глазного дна не менее одного раза в год), особенно в регионах, где служба специализированных кабинетов ДР развита недостаточно, а возможность фотографирования сетчатки есть только в специализированных центрах. Стандартизация алгоритма офтальмоскопии у пациентов с СД с фоторегистрацией глазного дна существенно повышает качество диагностики ДР [15].
Создание электронной базы данных с архивацией материалов должно стать следующим этапом в развитии помощи пациентам с ДР в РФ. Это расширит возможности оценки данных пациента в динамике, в том числе с целью заочных консультаций, дистанционного контроля и коммуникаций по оценке эффективности проводимого лечения.
В профилактике терминальных осложнений со стороны глаз при СД взаимодействие эндокринологов и офтальмологов остается наиболее сложным вопросом. Так, к офтальмологу пациент часто попадает, обращаясь самостоятельно по месту жительства, при этом обратная связь о выполнении лазерной коагуляции (ЛК) сетчатки и других видов лечения отсутствует. Отсутствие четкой маршрутизации пациентов не обеспечивает механизма обратной связи, что затрудняет мониторинг динамики осложнений и отслеживание клинических исходов. Это еще раз актуализирует необходимость преемственности с целью повышения качества оказания специализированной офтальмологической помощи пациентам с СД в РФ.
Диабетическая нефропатия, хроническая болезнь почек
При анализе динамики распространенности поражения почек при СД в 2013-2017 гг. по сравнению с более ранним периодом ФЦП следует учитывать несколько объективных 85 регионов Вологодская об л. Карелия Респ. Тамбовская обл. Ленинградская обл. Тверская обл. Санкт-Петербург г. Липецкая обл. Ярославская обл. Смоленская обл. Архангельская обл. Орловская обл. Тульская обл. Новгородская обл. Ненецкий АО Воронежская обл. Рязанская обл. Татарстан Респ. Курская обл. Свердловская обл. Оренбургская обл. Брянская обл. Севастополь г. Ивановская обл. Костромская обл. Забайкальский край Красноярский край Курганская обл. Белгородская обл. Мурманская обл. Адыгея Респ. Самарская обл. Коми Респ. Калужская обл. Калининградская обл. Башкортостан Респ. Мордовия Респ. Алтайский край Нижегородская обл. Московская обл. Владимирская обл. Челябинская обл. Омская обл. Крым Респ. Пензенская обл. Псковская обл. Ульяновская обл. Пермский край Кировская обл. Саратовская обл. Ханты-Мансийский АО Ямало-Ненецкий АО Тюменская обл. Краснодарский край Москва г. Иркутская обл. Карачаево-Черкесская Респ. Волгоградская обл. Новосибирская обл. Астраханская обл. Магаданская обл. Северная Осетия - Алания Чукотский АО Кемеровская обл. Томская обл. Приморский край Ростовская обл. Алтай Респ. Хакасия Респ. Марий Эл Респ. Амурская обл. Ставропольский край Калмыкия Респ. Кабардино-Балкарская Респ. Удмуртская Респ. Сахалинская обл. Саха (Якутия) Респ. Хабаровский край Камчатский край Чувашская Респ. Еврейская АО Бурятия Респ. Тыва Респ. Ингушетия Респ. Дагестан Респ. Чеченская Респ. факторов, важнейшим из которых является изменение критериев диагностики диабетической нефропатии (ДН). Именно в эти годы в РФ произошел переход от оценки альбуминурии (АУ) в качестве классического маркера ДН к учету уровня СКФ для верификации поражения почек при СД. Огромный пул пациентов со сниженной СКФ при нор- моальбуминурии, который не учитывался в диагнозе ДН, увеличил численность пациентов с этим осложнением по критериям ХБП.
Так, частота регистрации новых случаев ХБП в РФ возросла в 2017 г. по сравнению с 2013 г.: в 2,85 раза при СД1 (125,9-359,2 на 10 тыс. пациентов с СД1) и в 6,4 раза при СД2 (59,3-379,1 на 10 тыс. пациентов с СД2) при отсутствии истинного повышения частоты развития осложнения. При этом доля терминальной стадии ХБП (С5) среди всех случаев ХБП при СД1 и СД2 стабильно снижается (рис. 7).
Одним из ведущих факторов развития ХБП остается длительность СД: при длительности СД1 <5 лет ХБП развивается у 5,1% пациентов, при СД1 >30 лет - у 48,0%, при СД2 - у 3,5 и 20,3%, соответственно [16].
К сожалению, ни в одной из стран мира не удалось полностью остановить прогрессирование ХБП. Мировые и отечественные данные согласуются в том, что успехи в ведении пациентов с СД в последние годы не устраняют риск ХБП, но дают отсрочку в ее развитии. С целью профилактики прогрессирования ХБП до выраженных стадий тактика ранней диагностики, наряду с широким использованием средств блокады ренин-ангиотензиновой системы, остаются базовыми и наиболее эффективными методами нефропротекции при СД. В последние годы изучается нефропротективный потенциал современных сахароснижающих препаратов, в том числе агонистов глюкагоноподобного пептида и ингибиторов натрий-глюкозного котранспортера 2-го типа (глифлозинов).
Синдром диабетической стопы и ампутации
Изучение эпидемиологических характеристик СДС представляет особую актуальность, поскольку его развитие повышает риск ампутаций нижних конечностей, что ведет к потере трудоспособности, инвалидизации, снижению продолжительности жизни, а также повышению расходов общества на лечение.
Мировые данные по частоте ампутаций у пациентов с СД характеризуются высокой вариабельностью: от 46,1 до 9600 на 10 тыс. пациентов с СД, что значительно выше по сравнению с показателями в общей популяции - 5,8-31 на 100 тыс. человек [17]. Прогноз выживания пациентов с СДС, и особенно пациентов с СД после ампутаций нижних конечностей, значительно хуже, чем у больных с онкологическими заболеваниями [18]. При этом по стоимости лечения СДС представляет собой одну из наиболее затратных патологий при СД. Так, по данным Международной федерации диабета (IDF), лечение больных с СДС в 5 раз повышает стоимость расходов на лечение [6].
В связи с этим нам чрезвычайно важно констатировать значительное снижение распространенности СДС в РФ в динамике 2007-2017 гг. - в 1,5 раза при СД1 (с 6,3 до 4,3%) и в 3 раза при СД2 (с 5,1 до 1,7%; см. рис. 5 на цветной вклейке).
В последние годы отмечается тенденция к снижению распространенности СДС (рис. 8). Отмечается значительная межрегиональная вариабельность частоты ампутаций - от 0,13 до 2,9% у пациентов с СД1, от 0,04 до 6,0% у пациентов с СД2 [19]. Выраженные межрегиональные различия в частоте ампутаций могут отражать дисбаланс в качестве оказания специализированной помощи в регионах, в том числе отсутствие или нехватку кабинетов и отделений диабетической стопы в ряде субъектов РФ, что существенно влияет на эффективность профилактических мер в группах риска. Ведение пациентов с СДС в условиях общей хирургической практики без участия эндокринологов и специалистов-подиатров признано менее эффективной тактикой во всем мире, поскольку зачастую оно ограничивается именно хирургической помощью пациентам с уже развившимся осложнением.
Эти данные вызывают тревогу, поэтому требуется усиление мер по развитию специализированной помощи пациентам с СДС не только на федеральном уровне, но в региональных центрах диабета и в лечебных учреждениях третьего уровня субъектов РФ, которые обязательно должны иметь в своей структуре специализированные кабинеты диабетической стопы и возможность для проведения реконструктивных операций на сосудах нижних конечностей в условиях профильных отделений.
По данным Регистра, в последние 5 лет число ампутаций на 10 тыс. взрослых пациентов остается на прежнем уровне при обоих типах СД (см. рис. 8). Важно отметить, что при анализе уровня проведенных ампутаций отмечается стабильное снижение доли высоких ампутаций и перераспределение соотношения в пользу малых (сохраняющих опорную функцию стопы) хирургических вмешательств на ранних стадиях развития поражения нижних конечностей (рис. 9). Установлено, что прогноз жизни пациентов с СДС зависит именно от уровня ампутации. Так, средний срок выживания пациентов с СД с высокими ампутациями (на уровне бедра и голени) составляет 40 мес, что значимо ниже по сравнению с малыми оперативными вмешательствами (на уровне стопы и пальцев) - 51 мес (р=0,016) [20].
Поэтому в ряде европейских стран частота и уровень ампутаций у пациентов с СД служат не просто критерием качества организации специализированной помощи пациентам с данным видом осложнения, но рассматриваются как ключевой индикатор эффективности диабетологической помощи на национальном уровне. Таким образом, несмотря на сохраняющийся в динамике последних лет стабильный показатель частоты ампутаций в целом по РФ, отмечено снижение частоты высоких ампутаций, но увеличение числа минимальных ампутаций в пределах одного пальца, что отражает улучшение качества оказания помощи пациентам с СДС.
Сердечно-сосудистые заболевания
Актуальность изучения эпидемиологии сердечно-сосудистых заболеваний (ССЗ) не вызывает сомнений: ССЗ являются основной причиной смертности не только у пациентов с СД [21], но и в популяции в целом. Вопрос о том, является ли ССЗ осложнением СД или конкурирующей патологией, развивающейся параллельно СД или даже предшествующей его развитию, один из самых дискуссионных в современной диабетологии. Важно, что пациенты с сочетанием СД и клиническими исходами заболеваний системы кровообращения предоставляют собой одну из наиболее высоких категорий риска смертности.
Благодаря активным профилактическим программам и масштабному улучшению оказания медицинской помощи больным с ССЗ, внедрению новых методов диагностики и лечения в клиническую практику эпидемиологическая ситуация по ССЗ при СД значительно улучшилась. Среди наиболее важных факторов следует отметить появление препаратов, улучшающих клинический прогноз пациентов с ССЗ (блокаторы ренин-ангиотензин-альдостероновой системы, статины, антитромботические препараты). Второе, что не менее, а может быть и более важно, - действительно широкое, повсеместное применение этих препаратов в лечебной практике. Наконец, действительно мощное развитие сердечно-сосудистых центров, выполняющих реконструктивные операции на сосудах и оказывающих экстренную помощь больным с острыми формами ИБС и ЦВЗ. Такие центры появились в большинстве крупных городов субъектов РФ, что могло стать одним из ключевых факторов снижения в последние годы заболеваемости (новых случаев) ССЗ у больных СД1 и СД2 в РФ, выявленного по данным нашего исследования.
Успехи в снижении ССЗ достигнуты действительно впечатляющие. В динамике 10-летнего периода (2007-2017) частота ИМ при СД1 снизилась в 4,7 раза, при СД2 - в 2,2 раза (см. рис. 5 на цветной вклейке). В последние годы сохраняется снижение показателей как распространенности, так и заболеваемости ССЗ в РФ. Так, количество новых случаев в год ИМ уменьшилось с 10,8 до 8,0 на 10 тыс. взрослых пациентов при СД1, с 303 до 22,5 на 10 тыс. взрослых пациентов при СД2; ИБС - с 13,1 до 12,3 и с 58,3 до 42,5 на 10 тыс. взрослых пациентов, соответственно, ЦВЗ - с 13,6 до 12,7 при СД1, с 44,0 до 38,5 на 10 тыс. взрослых пациентов при СД2 (рис. 10). Отмечается увеличение длительности СД на момент развития как ИМ при обоих типах СД (на 2,4 года при СД1 и на 1,8 года при СД2), так и ЦВЗ (на 3,9 года при СД 1 и на 1,6 года при СД2) [22].
Риск развития макрососудистых заболеваний начинает повышаться уже на стадии предиабета [23]. Достижение целевого контроля гликемии у пациентов с СД достоверно снижает риск всех микрососудистых осложнений и в значительно меньшей степени влияет на развитие ССЗ, что обусловливает важнейшее значение негликемических факторов, таких как артериальная гипертензия, дислипидемия, ожирение, коррекция которых является важнейшим аспектом клинической тактики при ведении этих пациентов.
Таким образом, помимо контроля гликемии, успешное решение вопросов профилактики развития ССЗ требует мультифакторного подхода - антигипертензивной терапии препаратами с органопротективными эффектами, контроля показателей атерогенного спектра крови, а также изменения образа жизни пациента (отказа от курения, снижения избыточной массы тела, ограничения потребления соли, увеличения физической активности). Все эти аспекты вошли в состав государственных программ сердечно-сосудистой профилактики в РФ в последние годы.
Заключение
В результате работы регистра СД создана единая динамическая база данных в онлайн-формате, включающая 84 субъекта РФ, позволяющая обеспечивать учет и динамический мониторинг эпидемиологических показателей СД, оценивать качество оказания диабетологической помощи и принимать организационно-управленческие решения, направленные на повышение эффективности диабетологической службы в стране.
За последнее десятилетие в РФ достигнуто значимое снижение острых (комы) и хронических микро- и макрососудистых осложнений СД (в том числе слепоты, терминальных стадий ХБП, доли высоких ампутаций, распространенности ИБС и ЦВЗ, количества новых случаев ИМ), улучшилось качество диагностики осложнений на более ранних стадиях.
Ключевыми факторами данных достижений стали масштабные государственные меры в период действия подпрограммы ФЦП «Сахарный диабет» и в последующие годы, направленные на развитие диабетологической службы в РФ, создание специализированных кабинетов диабетической ретинопатии и диабетической стопы, «Школ диабета», внедрение структурированных программ обучения.
Оценка данных контроля углеводного обмена представляет огромное значение как в клиническом аспекте - для мониторинга эффективности сахароснижающей терапии и своевременного принятия решения о необходимости ее интенсификации, так и для анализа качества оказания диабетологической помощи. С этой целью повышение доступности исследования НЬАІс вне зависимости от места жительства пациента и увеличение кратности его измерения в соответствии со стандартами оказания специализированной диабетологической помощи является важнейшей задачей.
Можно выделить приоритетное направление дальнейшего развития диабетологической помощи в РФ, ориентированное на профилактику развития новых случаев потери зрения, ампутаций и терминальной ХБП, для достижения которого необходима стандартизация оказания первичной специализированной помощи, а также унификация алгоритмов обследования и методов ранней диагностики. Выраженные межрегиональные различия в частоте и исходах осложнений могут отражать дисбаланс в качестве оказания специализированной помощи в регионах. Решение этих проблем требует повышения мер по развитию специализированной помощи при СД не только на федеральном уровне, но, прежде всего, на уровне всех этапов оказания специализированной помощи в регионах - первичного звена, лечебных учреждений третьего уровня и региональных центров диабета в субъектах РФ.
ФГБУ «НМИЦ эндокринологии» выдвинул инициативу и обратился в Минздрав России с предложением сформировать в городах-миллионерах региональные эндокринологические центры, оснащенные самым необходимым для диагностики и лечения эндокринных заболеваний (прежде всего диабета и его осложнений). Пациенты будут иметь возможность «под одной крышей» получать всю необходимую помощь многопрофильной команды: эндокринолога, офтальмолога, кардиолога, невролога, нефролога, хирурга. В этом случае пациенту будет обеспечена полнота обследования и своевременная медицинская помощь, что поможет избежать развития тяжелых и необратимых сосудистых осложнений.
В свою очередь, постоянный мониторинг эпидемиологических показателей посредством качественного ведения регистра позволят повысить информативность получаемых данных и тем самым улучшить перспективы лечения пациентов с СД.
Благодарность. Авторы выражают благодарность ЗАО «Астон Консалтинг», обеспечивающей техническое сопровождение Федерального регистра сахарного диабета в онлайн-формате.
Работа выполнена в рамках исполнения государственного задания ФГБУ «Национальный медицинский исследовательский центр эндокринологии» Минздрава России.
Авторы заявляют об отсутствии конфликта интересов.
ЛИТЕРАТУРА/REFERENCES
- Дедов И .И., Шестакова М.В., Викулова О.К. Государственный регистр сахарного диабета в Российской Федерации: статус 2014 г. и перспективы развития. Сахарный диабет. 2015;18(3):5- 23 [Dedov П, Shestakova MV, Vikulova OK. National register of diabetes mellitus in Russian Federation: status on 2014. Sakharnyi Diabet - Diabetes Mellitus. 2015;18(3):5-23 (In Russ.)], doi: 10.14341/DM201535-22
- Дедов И.И., Шестакова M.B., Викулова OK. Эпидемиология сахарного диабета в Российской Федерации: клинико-статистический анализ по данным Федерального регистра сахарного диабета. Сахарный диабет. 2017;20(1):13-41 [Dedov П, Shestakova MV, Vikulova OK. Epidemiology of diabetes mellitus in Russian Federation: clinical and statistical report according to the federal diabetes registry. Sakharnyi Diabet - Diabetes Mellitus. 2017;20(l):13-41 (In Russ.)], doi: 10.14341/DM8664
- Дедов И.И., Шестакова M.B., редакторы. Результаты реализации подпрограммы «Сахарный диабет» Федеральной целевой программы «Предупреждение и борьба с социально значимыми заболеваниями. 2007-2012 годы». М., 2012 [Dedov П, Shestakova MV, editors. The results of the implementation of the “Diabetes mellitus" subprogram of the Federal target program “Prevention and control of socially significant diseases. 2007-2012. Moscow, 2012 (In Russ.)].
- Дедов ИЛ., Шестакова MB., Майоров А.Ю. и др., редакторы. Алгоритмы специализированной медицинской помощи больным сахарным диабетом. 8-й выл. Сахарный диабет. 2O17;2O(1S):1-121 [Dedov П, Shestakova MV, Mayorov AY, et al., eds. Standards of specialized diabetes care. 8th Sakharnyi Diabet - Diabetes Mellitus. 2O17;2O(1S):1-121 (In Russ.)], doi: 10.14341/DM8146
- gks ли [интернет]. Федеральная служба государственной статистики [доступ от 15.01.2019]. Доступно ссылке http://www.gks.ru. [gksхи [Internet]. Russian Federal State Statistics Service [cited 2019 Jan 15]. Available from: http://www.gks.ru. (In Russ.)].
- IDF Diabetes Atlas, 8th Brussels: International Diabetes Federation; 2017. Available from: https://www.idf.otg/e-library/epidemiology-research/diabetes-atlas/134-idf-diabetes-atlas-8th-edition.html
- The Swedish National Diabetes Register (NDR) 20 years of successful improvements. Available from: https://www.ndr.nu/# Layout and production: GCL 2016 (ndr.nu/pdfs/20yearsofsuccessfulimprovements.pdf).
- Дедов ИЛ., Шестакова MB., Г алстян Г В. Распространенность сахарного диабета 2 типа у взрослого населения России (исследование NATION). Сахарный диабет. 2016;19(2):104-12 [Dedov П, Shestakova MV, Galstyan GR. The prevalence of type 2 diabetes mellitus in the adult population of Russia (NATION study). Sakharnyi Diabet - Diabetes Mellitus. 2016;19(2):104-12 (In Russ.)]. doi: 10.14341/DM2004116-17
- Майоров A.10., Викулова O.K., Железнякова AB. и др. Эпидемиология острых осложнений (комы) по данным Федерального регистра больных сахарным диабетом Российской Федерации (2013-2016 гг.). Сахарный диабет. 2018;21(6):444-54 [Mayorov AYu, Vikulova OK, Zheleznyakova AV, et al. Epidemiology of acute diabetes complications (coma) according to the Federal Diabetes register of the Russian Federation (2013-2016). Sakharnyi Diabet - Diabetes Mellitus. 2018;21(6):444-54 (In Russ.)], doi: 10.14341/DM10028
- Karges В, Rosenbauer J, Kapellen T, et al. Hemoglobin Ale Levels and risk of severe hypoglycemia in children and young adults with type 1 diabetes from Germany and Austria: a trend analysis in a cohort of 37,539 patients between 1995 and 2012. PLoS Med. 2014 Oct 7;ll(10):el001742. doi: 10.1371/joumal.pmed.l001742
- Hypoglycaemia Study Group: Risk of hypoglycaemia in types 1 and 2 diabetes: effects of treatment modalities and their duration. Diabe- tologia. 2007;50:1140-7.
- Старостина Е.Г. Гипогликемия и гипогликемическая кома. Медицинский совет. 2013;(5-6):6-10 [Starostina EG. Hypoglycemia and hypoglycemic coma. Meditsinskiy Sovet. 2013;(5-6):6-10 (In Russ.)].
- Zhong VW, Juhaeri J, Cole SR, et al. Incidence and Trends in Hypoglycemia Hospitalization in Adults With Type 1 and Type 2 Diabetes in England, 1998-2013: A Retrospective Cohort Study. Diabetes Care. 2017;40(12):1651-60. doi: 10.2337/dcl6-2680
- Липатов Д.В., Викулова OK., Железнякова АВ. и др. Эпидемиология диабетической ретинопатии в Российской Федерации по данным Федерального регистра пациентов с сахарным диабетом (2013-2016 гг.). Сахарный диабет. 2018;21(4):230-40 [Lipatov DV, Vikulova OK, Zheleznyakova AV, et al. Trends in the epidemiology of diabetic retinopathy in Russian Federation according to the Federal Diabetes Register (2013-2016). Sakharnyi Diabet - Diabetes Mellitus. 2018;21(4):230-40 (In Russ.)], doi: 10.14341/DM9797
- Смирнова O.M. Диабетическая ретинопатия. Результаты международных многоцентровых исследований. Сахарный диабет. 2010;13(1):82—7 [Smirnova ОМ. Diabetic retinopathy. Results of international multicentre studies. Sakharnyi Diabet - Diabetes Mellitus. 2010;13(l):82-7 (In Russ.)].
- Шамхалова MJIL, Викулова OK., Железнякова AB. и др. Эпидемиология хронической болезни почек в Российской Федерации по данным Федерального регистра взрослых пациентов с сахарным диабетом (2013-2016 гг.). Сахарный диабет. 2018;21(3):160-9 [Shamkhalova MS, Vikulova OK, Zheleznyakova AV, et al. Trends in the epidemiology of chronic kidney disease in Russian Federation according to the Federal Diabetes Register (2013-2016). Sakharnyi Diabet - Diabetes Mellitus. 2018;21(3): 160-9 (In Russ.)], doi: 10.14341/DM9687
- Moxey PW, Gogalniceanu P, Hinchlife RJ, et al. Lower extremity amputations - a review of global variability in incidence. Diabet Med. Oct;28(10): 1144-53. doi: 10.1111 /j .1464-5491.2011,03279.x
- Hoffmann M, Kujath P, Flemming A, et al. Survival of diabetes patients with major amputation is comparable to malignant disease. Diabetes Vase Dis Res. 2015;12(4):265-71. doi: 10.1177/ 1479164115579005
- Галстян Г В., Викулова О.К., Исаков МА. и др. Эпидемиология синдрома диабетической стопы и ампутаций нижних конечностей в Российской Федерации по данным Федерального регистра больных сахарным диабетом (2013-2016 гг.). Сахарный диабет. 2018;21(3):170-7 [Galstyan GR, Vikulova OK, Isakov MA, et al.
- Trends in the epidemiology of diabetic foot and lower limb amputations in Russian Federation according to the Federal Diabetes Register (2013- 2016). Sakhamyi Diabet - Diabetes Mellitus. 2018;21(3):170-7 (In Russ.)], doi: 10.14341/DM9688
- Larsson J, Agardh C, Apelquist J, et al. Long-term prognosis after healed amputation in patients with diabetes. Clin Orthop Relat Res. 1998;350:149-58.
- Дедов И.И., Шестакова M.B., Викулова O.K., Железнякова А.В., Исаков М.А. Сахарный диабет в Российской Федерации: распространенность, заболеваемость, смертность, параметры углеводного обмена и структура сахароснижающей терапии по данным Федерального регистра сахарного диабета, статус 2017 г. Сахарный диабет. 2018; 21(3):144-59 [Dedov II, Shestakova MV, Vikulova OK, Zheleznyakova AA, Isakov MA. Diabetes mellitus in Russian Federation: prevalence, morbidity, mortality, parameters of glycaemic control and structure of hypoglycaemic therapy according to the Federal Diabetes Register, status 2017. Sakhamyi Diabet - Diabetes Mellitus. 2018;21(3):144-59 (In Russ.)], doi: 10.14341/DM9686
- Калашников В.Ю., Викулова OX., Железнякова AB., Исаков М.А. Эпидемиология сердечно-сосудистых заболеваний у больных сахарным диабетом по данным Федерального регистра Российской Федерации (2013-2016гг.). Сахарный диабет. 2019;22(3):epub [Kalashnikov VYu, Vikulova OK, Zheleznyakova AA, Isakov MA. Epidemiology of cardiovascular diseases (CVD) among patients with diabetes mellitus (DM), according to the Federal Diabetes register of the Russian Federation (2013-2016). Sakhamyi Diabet - Diabetes Mellitus. 2019;22(3):epub. (In Russ.)].
- Глобальный доклад по диабету. Женева: Всемирная организация здравоохранения; 2018. Лицензия: СС BY-NC-SA 3.0 IGO [Global report on diabetes. Geneva: World Health Organization, 2018. License: CC BY-NC-SA 3].





