Сахарный диабет: развитие технологий в диагностике, лечении и профилактике


Published: March 1, 2010
Latest article update: Nov. 22, 2022
Abstract
Сахарный диабет (СД) является одной из серьезнейших медико-социальных и экономических проблем здравоохранения всех стран мира.Наибольшая опасность этого заболевания связана с развитием сосудистых осложнений.Современный уровень диагностических средств, новейшие средства мониторинга гликемии, внедрение инновационных инсулинов и саха-роснижающих препаратов, развитие высокотехнологичных методов лечения может значительно изменить ситуацию в отношении про-гноза пациентов, снижения частоты развития, инвалидизации и смертности вследствие хронических осложнений СД.Поддержание целевого контроля факторов риска: гликемии, гипертонии и дислипидемии непосредственно с дебюта СД на протяжениивсей жизни пациента по-прежнему остается наиболее перспективным направлением профилактики развития и прогрессирования диа-бетических осложнений. Непреложным условием эффективного контроля СД является создание программ активного скрининга, на-правленных на максимально раннюю диагностику осложнений, и оптимальная организация клинико-диагностического процесса в рамкахобеспечения мультидисциплинарного подхода в лечении.
Keywords
Синдром диабетической стопы, сахарный диабет, Федеральная программа, диабетические осложнения, нефропатия, кардиальная патология, ретинопатия
Cахарный диабет (СД) представляет собой реальную угрозу здоровью и качеству жизни населения всех стран мира, являясь одним из наиболее распространенных хронических заболеваний. Сосудистые осложнения СД (микро- и макроангиопатии), такие как нефропатия, ретинопатия, поражение магистральных сосудов сердца, мозга, нижних конечностей, ежегодно приковывают к инвалидному креслу и уносят жизни миллионов человек, страдающих этим заболеванием. Такой широкий спектр осложнений, развивающихся при СД, объясняет столь высокий интерес к проблеме и участие в лечении этих больных не только эндокринологов-диабетологов, но и специалистов практически всех медицинских направлений: терапевтов и кардиологов, нефрологов и урологов, неврологов, гинекологов, окулистов, хирургов, семейных врачей.
ЭПИДЕМИОЛОГИЯ
Заболеваемость СД на земном шаре удваивается каждые 10-15 лет, приобретая характер неинфекционной эпидемии. По данным ВОЗ, в настоящее время в мире насчитывается 285 млн больных СД, а к 2025 г. их количество составит 380 млн и 435 млн – в 2030 г. При этом реальные темпы прироста заболеваемости значительно опережают даже столь удручающие прогнозы статистиков. Так, в 2000 г. количество больных СД оказалось на 11% больше – 175 млн против 154 млн по расчетным данным 1998 г.
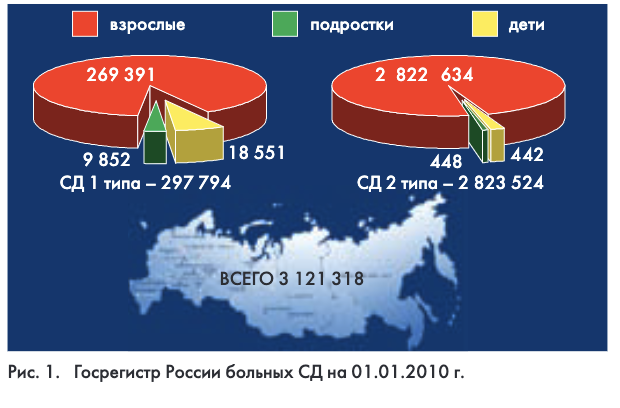
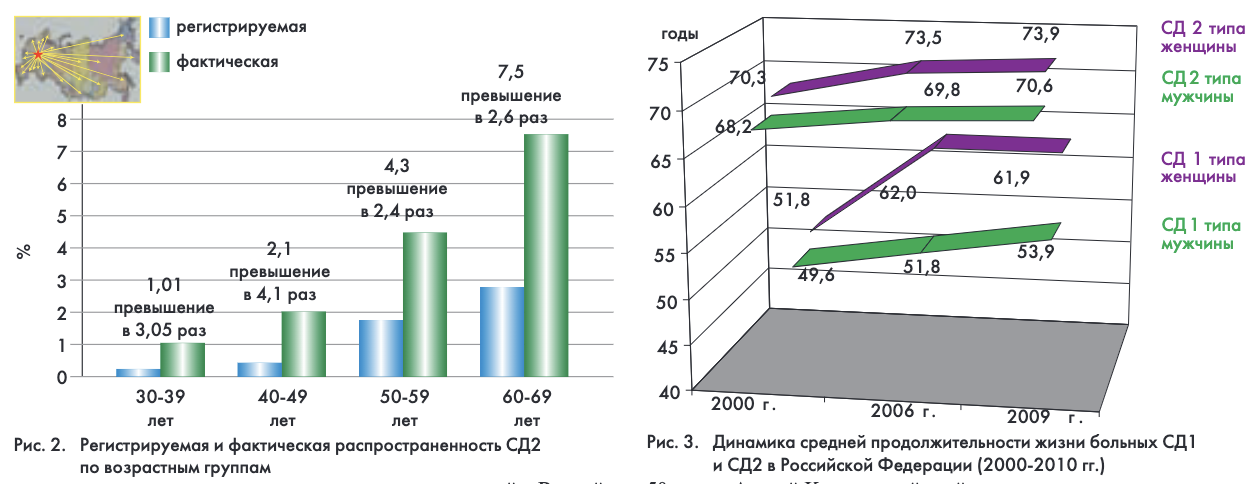
В России на 01.01.2010 г. зарегистрировано 3 121 318 больных СД, что составило 2 156 человек на 100 тыс. населения, из них 297 794 – больные СД 1 типа (СД1) и 2 823 524 – больные СД 2 типа (СД2) (рис. 1). Только за последнее десятилетие количество больных диабетом в России увеличилось более чем на 1 млн человек, однако истинная распространенность заболевания в 2-3 раза выше, преимущественно за счет СД2, что соответствует 6-9 млн больных (рис. 2).
Всемирная организация здравоохранения (ВОЗ), Международная диабетическая федерация и Сент-Винсентская декларация определили СД как эпидемическое заболевание неинфекционной природы и призвали правительства всех стран мира создать национальные программы для борьбы с этим заболеванием. В соответствии с решениями ведущих мировых организаций в Российской Федерации была разработана и в период 1996 – 2006 гг. реализована Федеральная целевая программа «Сахарный диабет» в рамках Федеральной целевой программы «Предупреждение и борьба с заболеваниями социального характера». Программа придала мощный импульс развитию диабетологической службы в стране. Все мы были ее участниками и теперь можем подвести определенные итоги.
За годы работы Программы в России создано более 100 региональных диабетологических центров с обязательным выделением профильных служб для обеспечения профилактики и лечения осложнений СД: кабинетов врача-диабетолога, кабинетов «Диабетическая стопа», диабетической ретинопатии, отделений и кабинетов кардиологии, отделений гемодиализа, кабинетов «Диабет и беременность», школ для больных СД и родителей больных детей.
Особое внимание обращалось на гарантированное обеспечение государством больных СД высококачественными инсулинами и средствами их введения, современными таблетированными сахароснижающими препаратами, средствами самоконтроля.
Создан Государственный регистр больных СД.
Организована система по профилактике СД, включая развитие санитарно-реабилитационных центров, организацию санитарно-просветительской работы среди населения и формирование групп риска с обучением и последующим динамическим наблюдением.
Средняя продолжительность жизни (СПЖ) больных СД – один из важнейших показателей эффективности лечебно-профилактической помощи пациентам. Проведенные расчеты показали, что за период 2000 – 2009 гг. СПЖ больных СД1 увеличилась на 4,3 года у мужчин и на 10,1 лет у женщин, больных СД2 – на 2,4 и 3,6 года соответственно, и превысила среднюю продолжительность жизни населения РФ (рис. 3). За последние десятилетия изменились и причины смертности при СД: значимо снизилась смертность больных от острых осложнений СД (комы) и, с другой стороны, в общей структуре смертности до 50-60% возросла доля сердечно-сосудистой патологии.
ИСТОРИЯ САХАРНОГО ДИАБЕТА: ТЕРМИНОЛОГИЯ И КЛАССИФИКАЦИИ
СД поистине является заболеванием цивилизации и сопровождает человечество на протяжении всей истории его развития. История этого заболевания насчитывает более 3,5 тысяч лет: 1500 лет до н.э. в папирусе Эберса диабет описан как состояние, сопровождающееся обильным выделением мочи. В 30-50 гг. н.э. Аретей Каппадокийский дал первое клиническое описание болезни. Сравнивая болезнь с «прохождением воды по сифону», дал ей название «диабет» (от греч. «диабайно» – проходить через, протекать). Термин «сахарный» – от лат. mellitus – «сладкий, медовый» – добавлен в XVII в. Томасом Уиллисом. Первая попытка классифицировать диабет предпринята в 1880 г. Lancereaux E. – он выделил два типа СД: легко поддающийся диетотерапии (diabete gras) и быстро прогрессирующий, резистентный ко всякому лечению (diabete maigre).
По мере совершенствования знаний о патогенезе заболевания нескольким пересмотрам подверглась классификация СД экспертов ВОЗ. Так, в 1965 г. ВОЗ выделяет: 1) первичный (эссенциальный) СД с фазами относительной и абсолютной инсулиновой недостаточности и 2) вторичный СД. В 1980 г. вводятся термины «диабет I типа» и «диабет II типа», а в 1985 г. эти термины вновь упраздняются, поскольку они предполагают доказанный патогенез заболевания, и принимается классификация, основанная на клинических классах: инсулинозависимый (ИЗД) и инсулиннезависимый (ИНЗД) диабет, нарушенная толерантность к глюкозе (НТГ) и СД беременных, а также впервые выделяются классы статистического риска. Наконец, в 1999 г. принимается современная – этиологическая классификация ВОЗ, которая используется до настоящего времени.
РАЗВИТИЕ КРИТЕРИЕВ ДИАГНОСТИКИ СД
Вторая половина XX в. стала периодом стремительного развития методов диагностики СД, разработки скрининговых программ, создания единых критериев диагностики, развития иммунологических и генетических методов дифференциальной диагностики различных типов СД.
Проблемы скрининга СД, а именно: поздняя диагностика СД2, когда до 25% пациентов с впервые выявленным СД уже имеют микрососудистые осложнения, что свидетельствует о его длительном скрытом течении, дважды за последние 20 лет послужили причиной изменения критериев диагностики заболевания.
- В 1997 г. Американской диабетической ассоциацией (АДА) предложено и в 1999 г. одобрено ВОЗ снизить диагностический порог СД при исследовании гликемии натощак с 7,8 до 7,0 ммоль/л.
- Включение показателя гликированного гемоглобина (HbA1c≥6,5%) в качестве критерия диагностики СД (Международный экспертный комитет, 1999 г. и АДА, 2010 г.).
Согласно современным критериям, диагностика СД может проводиться любым из доступных методов: гликемия натощак ≥7,0 ммоль/л, гликемия через 2 часа при пероральном тесте толерантности к глюкозе (ПТТГ) ≥11,1 ммоль/л, случайной гипергликемии ≥11,1 ммоль/л при наличии симптомов или HbA1c≥6,5%. Для верификации диагноза обязательно наличие любых 2-х из указанных критериев или двукратное подтверждение одного.
РАЗВИТИЕ СРЕДСТВ ЛЕЧЕНИЯ СД
В лечении СД совершенно четко можно выделить две эпохи. В доинсулиновую эпоху диагноз «СД» практически не оставлял больному шансов на выживание: смерть вследствие кетоацидоза в 90% случаев, продолжительность жизни не более двух-трех лет.
ХХ в. становится по-настоящему прорывным в истории диабетологии, периодом бурного развития знаний о патогенезе и этиологии СД, стремительного совершенствования инсулинов и средств их введения, создания новых сахароснижающих препаратов.
ИНСУЛИНЫ
В 1921 г. Banting F.G. и Best H.С. (кафедра профессора McLeod J.J.R.) выделили инсулин из поджелудочной железы теленка. Введение препарата панкреатэктомированной собаке с клиническими проявлениями СД привело к нормализации уровня гликемии. Это открытие, за которое McLeod J.J.R. и Banting F.G. получили Нобелевскую премию по медицине в 1923 г., послужило началом новой «инсулиновой» эпохи в лечении СД.
Уже год спустя – в 1922 г. – Joslin E.P. с успехом применил первые препараты животного инсулина в клинической практике. В 1926 г. Abel J.J. получил кристаллическую форму инсулина. 1940-е гг. ознаменованы разработкой инсулина НПХ (нейтрального протамина Хагедорна), 1950-е – разработкой инсулинов типа Ленте.
Совершенствовались не только технологии производства инсулина. По мере накопления знаний о причинах развития диабетических осложнений изменялись и принципы инсулинотерапии.
1970-е гг. – данные о более высоком риске микрососудистой патологии на фоне традиционной инсулинотерапии с использованием одно- или двукратных инъекций инсулина послужили предпосылкой для пересмотра принципов инсулинотерапии и разработки базис-болюсной концепции и интенсивной инсулинотерапии как наиболее эффективного способа коррекции углеводного обмена.
1977 – 78 гг. – расшифровка структуры гена инсулина.
1980-е гг. – использование рекомбинантной ДНК-технологии для производства человеческих инсулинов. Появление инсулиновых шприц-ручек.
1990-е гг. – большое количество исследований продемонстрировало эффективность предупреждения микро- и макрососудистых осложнений СД на фоне поддержания уровня гликемии, близкого к нормальному. Разработка аналогов инсулина ультракороткого действия (ЛизПро, Аспарт, Глулизин).
2000-е гг. – разработка аналогов инсулина длительного беспикового действия (Гларгин, Детемир). Появление современных инсулиновых дозаторов (помп). Помпы 4-го поколения с интегрированными устройствами для непрерывного мониторирования концентрации глюкозы позволяют не просто вводить инсулин в соответствии с настройками, но и снабжены программами автоматического расчета дозы инсулина и способны самостоятельно менять дозу инсулина в ответ на изменения концентрации глюкозы (например, отключать подачу инсулина при гипогликемии).
Таким образом, менее чем за сто лет, прошедших со времени открытия инсулина, достигнут беспрецедентный по своей значимости прогресс: от полного отсутствия средств лечения СД1 до возможности имитировать физиологическую секрецию и поддерживать нормогликемию при помощи помповой инсулинотерапии с использованием аналогов инсулина человека!
САХАРОСНИЖАЮЩИЕ ПРЕПАРАТЫ
Конец 20-х гг. – начало клинического изучения препарата из группы бигуанидов синталина. 1957 г., Unger R. – синтез фенформина. 1942 г., Janbon M. – первое сообщение о сахароснижающем действии производных сульфонилмочевины (СМ). 1956 г. – синтез СМ первой генерации (надизан, оранил, карбутамид, толбутамид). В 1966 г. синтезированы препараты второй генерации (глибенкламид).
1990 гг. – широкое использование сахароснижающих препаратов, уменьшающих инсулинорезистентность (метформин) и сульфонилмочевины нового поколения (гликлазид МВ, глимепирид). В отличие от глибенкламида, препараты СМ последнего поколения влияют на первую фазу секреции инсулина и обеспечивают более выраженное снижение пика гипергликемии после приема пищи, а также могут применяться у пациентов с диабетической нефропатией (при скорости фильтрации <60 мл/мин/1,73 м2).
2005-2009 гг. – последовательно появились две новые группы препаратов, влияющих на систему инкретинов – гормонов желудочно-кишечного тракта, которые стимулируют секрецию инсулина (особенно первую фазу секреции инсулина): агонисты глюкагоноподобного пептида-1 (эксенатид, лираглутид) и ингибиторы дипептидилпептидазы-4 (ДПП-4) (ситаглиптин, вилдаглиптин, саксаглиптин). В результате комплексного действия этих препаратов происходит выраженное снижение сахара крови после приемов пищи без увеличения риска гипогликемий. Дополнительное преимущество – снижение веса.
РАЗВИТИЕ СРЕДСТВ САМОКОНТРОЛЯ И ОБУЧЕНИЕ ПАЦИЕНТОВ
Со времен метода Гиппократа – качественного определения глюкозурии (на вкус) средства контроля СД прошли огромный путь развития. В 1913 г. Bang J. (1869–1918) впервые предложил методику количественного определения содержания сахара в крови. Совсем недавно, еще в 70-80-е гг. XX в. в России единственным доступным способом контроля диабета были разовые исследования сахара крови лабораторным методом в условиях стационара или поликлиники. Результат гликемии получали постфактум, что не давало возможности оценки истинных показателей углеводного обмена и адекватной коррекции терапии, да и воспользоваться этим методом пациент мог отнюдь не часто. Давно стали достоянием истории и визуальные тест-полоски неколичественного определения гликемии и глюкозурии.
В настоящее время у больного диабетом имеется широкий выбор современных индивидуальных глюкометров, позволяющих в течение нескольких секунд получить точный результат гликемии в любой момент времени, что дает возможность адаптировать прием углеводов и дозу инсулина, планировать физическую активность, а следовательно, лучше контролировать свое заболевание.
В 1970-е гг. разработан и в течение последних 20-ти лет повсеместно внедрен в клиническую практику метод исследования гликированного гемоглобина (HbA1c) – интегрального показателя компенсации, отражающего средние показатели гликемии за предыдущие 90-120 дней (период полужизни эритроцитов). Этот метод стал незаменим для оценки эффективности проводимой терапии и риска развития осложнений. Последнее десятилетие ознаменовалось разработкой новейших способов контроля СД. Система непрерывного мониторирования концентрации глюкозы (CGMS) при помощи сенсора, установленного в подкожной жировой клетчатке живота, позволяет получить полный гликемический профиль пациента в течение нескольких суток, дает возможность графического изображения результатов и расчета количества измерений в пределах целевых значений.
Новейшая модификация системы непрерывного мониторирования концентрации глюкозы (Guardian Real-Time и Paradigm Real-Time, интегрированная в помпу) определяет концентрацию глюкозы в конкретный момент времени, что позволяет максимально быстро реагировать на ситуацию, предупреждать, а не купировать гипо- и гипергликемию и добиваться практически идеальных показателей углеводного обмена.
Однако ни один, даже самый современный метод контроля гликемии, не дает гарантии достижения компенсации СД без соответствующего обучения пациентов.
С 1998 г. после доклада экспертов ВОЗ «Терапевтическое обучение больных» СД причислен к заболеваниям, при которых обучение пациентов является одним из обязательных и наиважнейших аспектов лечения. Целью процесса обучения является создание у пациента мотивации к активному управлению своим заболеванием в союзе с врачом на основе полученных знаний и практических навыков.
За последние 20 лет, в том числе в рамках реализации программы «Сахарный диабет», в России создана единая методологическая база обучения в диабетологии, разработаны и внедрены специализированные структурированные программы обучения пациентов, организовано более 1000 «Школ для больных СД» в различных регионах РФ, создана система подготовки кадров в этой области. Важнейшей функциональной единицей в процессе обучения являются «Школы для больных СД» с привлечением мультидисциплинарной команды, состоящей из врачей, среднего медперсонала, диетолога и психолога.
Многолетний опыт обучения и динамического наблюдения пациентов в отделении «Обучения и психосоциальной реабилитации» ФГУ ЭНЦ позволяет говорить о высокой эффективности данного подхода, о чем свидетельствует значимое и стабильное снижение уровня HbA1c у пациентов, прошедших обучение, полное отсутствие диабетических ком, снижение частоты микроангиопатий, потребности и продолжительности госпитализаций, связанных с диабетом и осложнениями.
ОСЛОЖНЕНИЯ СД
ДИАБЕТИЧЕСКАЯ РЕТИНОПАТИЯ
Диабетическая ретинопатия (ДР) занимает особое место среди осложнений СД, поскольку значительно снижает качество жизни пациентов, вызывая прогрессирующее снижение или полную потерю зрения. Слепота у больных СД развивается в 25 раз чаще, чем в общей популяции.
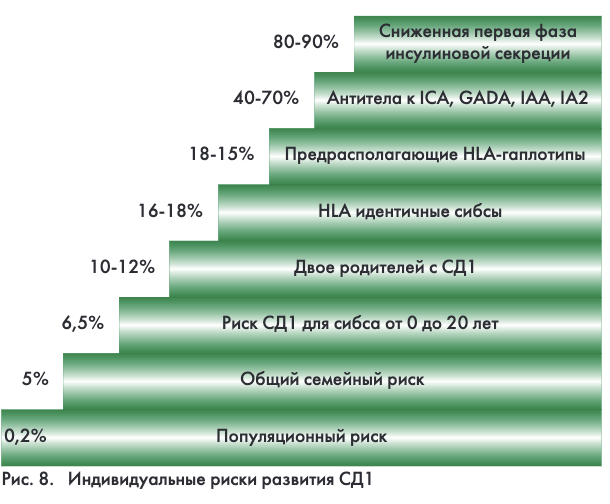
Распространенность ДР чрезвычайно высока: при СД1 с длительностью заболевания более 10-15 лет это осложнение диагностируется у 80–90% пациентов, из них у 30% – пролиферативная стадия ДР. При СД2 ДР выявляется у 7–20% пациентов уже в дебюте заболевания и достигает 70–80% при длительности СД более 20 лет.
Впервые это осложнение было описано более 100 лет назад – в 1879 г. MacKenzie. За этот период клинические признаки и факторы развития ДР очень хорошо изучены. Несомненно, что ведущую роль в развитии и прогрессировании ДР играет гипергликемия. Результаты основополагающих исследований дают нам однозначный ответ: при достижении целевых показателей HbA1c развитие ДР можно предупредить или значительно замедлить: у больных СД1 – снижение риска развития ДР на 76% и риска прогрессирования на 53–64% (DCCT), у больных СД2 типа – на 21% в течение 12 лет (UKPDS). Поэтому все возможные усилия в профилактике и лечении этого осложнения в первую очередь должны быть направлены на коррекцию углеводного обмена. В этой связи особенно опасно мнение некоторых врачей, что при уже развившейся ДР и выраженной декомпенсации углеводного обмена не следует стремиться к достижению целевых значений гликемии. Действительно, доказана возможность появления новых кровоизлияний после гипогликемий. Однако это еще раз подтверждает необходимость поддержания стабильных показателей гликемии с постепенным снижением уровня HbA1c примерно на 1% в месяц.
Сегодня в арсенале врачей-офтальмологов имеются огромные возможности ранней диагностики патологии органа зрения при СД: прямая и непрямая офтальмоскопия, гониоскопия, стереоскопическое фотографирование стандартных полей сетчатки, сканирующая лазерная офтальмоскопия, оптическая когерентная томография (ОКТ), флуоресцентная ангиография (ФАГ).
Однако, несмотря на многообразие методов диагностики ДР, у 20% пациентов осложнение выявляется уже на пролиферативной стадии. Важно помнить, что даже выраженные диабетические изменения глазного дна могут не нарушать остроту зрения. Больной не имеет жалоб и не обращается к офтальмологу самостоятельно. Обеспечение систематического офтальмологического наблюдения всех пациентов с СД является прямой обязанностью лечащего эндокринолога-диабетолога. Пациенты с СД2 должны направляться на первичный осмотр офтальмологом непосредственно при установлении диагноза, пациенты с СД1 – при длительности диабета более 3-х лет. Повторные осмотры необходимы при отсутствии патологии не реже 1 раза в год, при непролиферативной ДР – 2 раза в год, при пре- или пролиферативной ДР – 1 раз в 3-4 месяца.
Проблема предупреждения слепоты вследствие диабетической патологии глаз во многом носит организационный характер и требует: четкого взаимодействия врачей различных специальностей и своевременного направления пациента к офтальмологу с целью адекватного офтальмологического обследования и своевременного начала лечения. Абсолютно необходимым для осуществления этой задачи является создание системы «кабинетов ретинопатии» в качестве первичного звена и специализированных отделений на базе диабетологических центров с наличием соответствующего оборудования и специалистов для оказания высокотехнологичной офтальмологической помощи.
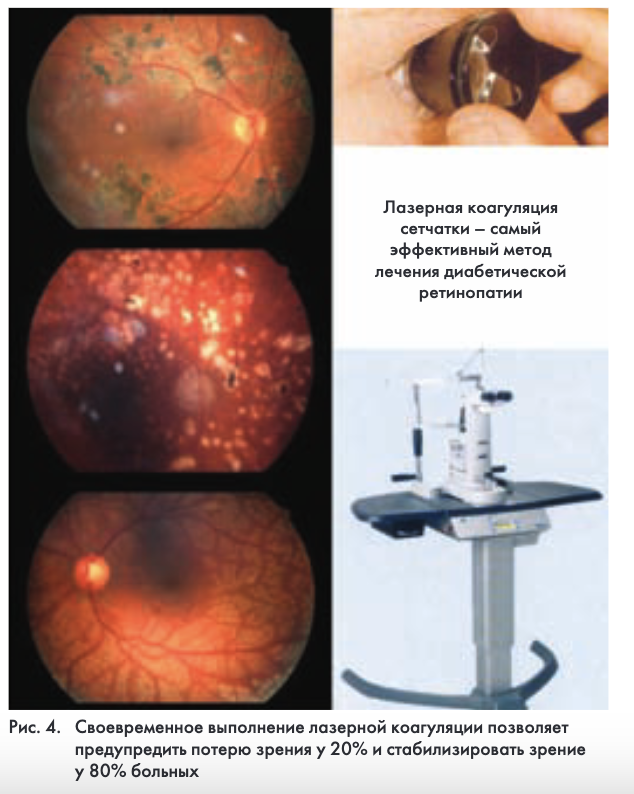
Всемирно признанным методом лечения ДР является лазерная фотокоагуляция (ЛФК) сетчатки. Впервые она была выполнена более 40 лет назад – в 1959 г. Meyer-Schwickerath. Однако и в настоящее время ЛФК остается единственным эффективным методом лечения ДР (рис. 4). Многолетний опыт лечения и наблюдения пациентов с ДР в офтальмологическом отделении ФГУ ЭНЦ позволяет с уверенностью говорить, что эффективность ЛФК сетчатки составляет: 94% – при непролиферативной стадии ДР, 90% – при препролиферативной и 80% – при пролиферативной ДР. При развитии грубых изменений сетчатки и стекловидного тела (витреоретинальных тяжей и отслойки) методом выбора является витреоретинальная хирургия.
По мнению экспертов ВОЗ, в настоящее время не существует лекарственных препаратов, способных конкурировать по эффективности с лазерными методами лечения ДР. Тем не менее в последние годы появилось новое перспективное направление развития консервативной терапии ДР – интравитреальные инъекции кристаллических кортикостероидов и ингибиторов ангиогенеза, введение которых в дополнение к ЛФК позволяет улучшить результаты лечения. В отношении эффективности применения этих препаратов изолированно, без ЛФК, необходимо проведение дальнейших исследований.
Наиболее перспективным направлением предупреждения терминальных осложнений, ведущих к потере зрения, остается коррекция факторов риска (контроль гипергликемии, гипертонии, дислипидемии) и обеспечение эффективных программ активного скрининга, направленного на выявление и лечение начальных стадий ДР.
ДИАБЕТИЧЕСКАЯ НЕФРОПАТИЯ
Проблема диабетической нефропатии (ДН) появилась в начале ХХ в. Еще в 1936 г. Kimmelstiel P. и Wilson С. дали первое классическое описание поражения почек при длительном течении СД. За истекшие десятилетия достигнут огромный прогресс в понимании природы этого осложнения, механизмов его развития и методов воздействия на них.
Однако, несмотря на все достигнутые успехи, о решении проблемы этого осложнения СД говорить не приходится. Во всем мире терминальная хроническая почечная недостаточность (тХПН), развившаяся вследствие ДН, остается лидирующей причиной смертности больных СД1. У больных СД2 ДН занимает 2-е место среди причин смерти после сердечно-сосудистых заболеваний. ДН по-прежнему рассматривают как прогрессирующее и необратимое (при развитии ПУ) поражение почек при СД.
Распространенность ДН достигает 40-50% вне зависимости от типа СД. При длительности СД 10–15 лет частота ДН составляет 15–20%, 20 лет – 20–35% и при более длительном течении СД – до 50%. По данным эпидемиологических исследований в рамках программы «Сахарный диабет» в 20 регионах РФ средняя частота ДН при СД1 составила 41,9%, при СД2 – 40,6%. При этом выявленная при активном скрининге частота осложнения в 2-3 раза превышала регистрируемую частоту патологии по данным локальных регистров, прежде всего, за счет недостаточной диагностики начальной стадии микроальбуминурии (МАУ). К сожалению, в России, как и во многих странах мира, диагностика и профилактика ДН идут с определенным опозданием, что и приводит к необратимым последствиям.
Выявление ДН на начальной стадии МАУ имеет определяющее прогностическое значение для прогноза пациента, поскольку данная стадия является потенциально обратимой. МАУ не выявляется при помощи рутинных методов обследования и требует использования специальных методик исследования мочи. В настоящее время доступен широкий выбор качественных диагностикумов для определения МАУ: лабораторные иммунохимические и радиоиммунологические методы, экспресс-анализаторы, которые в течение нескольких минут позволяют получить количественный результат, наконец, визуальные тест-полоски для исследования МАУ неколичественным способом. Тем не менее у 20-30% пациентов ДН впервые диагностируется на более выраженных стадиях – протеинурии (ПУ) и даже ХПН. Причина заключается в невыполнении этого исследования или в несоблюдении необходимых для выявления начальной стадии сроков скрининга.
Основой первичной профилактики ДН, как и других диабетических осложнений, является поддержание целевых показателей гликемии. По данным исследований UKPDS и DCCT, риск развития ДН можно значительно снизить: при СД2 – на 35%, при СД1 – МАУ на 39%, ПУ – на 54%.
Основной принцип лечения ДН – комплексная терапия, направленная на коррекцию всех возможных факторов поражения почек: компенсацию углеводного обмена, назначение препаратов нефропротективного действия, начиная со стадии МАУ вне зависимости от наличия гипертонии, целевой контроль АД (<130/80 мм рт.ст.), ограничение потребления животного белка, коррекцию дислипидемии, коррекцию анемии, гиперкалиемии, нарушений фосфорно-кальциевого обмена.
Такой комплексный подход значительно замедляет темпы прогрессирования патологии, а на начальной стадии ДН позволяет в 50% случаев добиться регресса МАУ и восстановления нормальных показателей функционального состояния почек. Так, первые исследования 80-90-х гг. ХХ в. показали, что примерно 80% больных СД1 с МАУ прогрессируют до стадии ПУ за 6–14 лет. Более поздние данные демонстрируют, что в течение 10 лет ПУ развивается у 35–40% пациентов с МАУ, что является свидетельством высокой эффективности программ интенсивного контроля гликемии, АД и нефропротективной терапии у больных с ДН, особенно на начальной стадии.
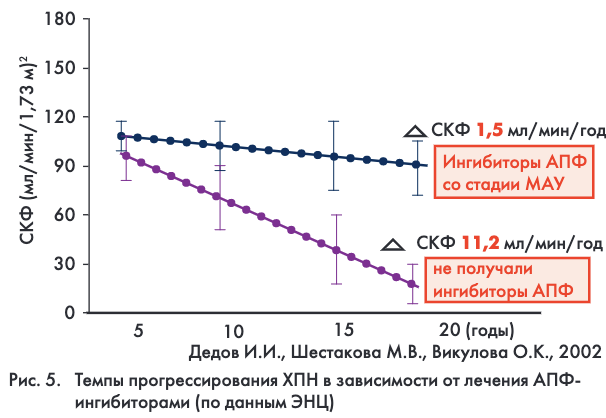
В настоящее время препараты, блокирующие ренин-ангиотензиновую систему (РАС): ингибиторы ангиотензин-превращающего фермента (иАПФ) и блокаторы рецепторов ангиотензина II (БРА) сохраняют лидирующие позиции в качестве средств патогенетической терапии ДН. Эти препараты более эффективно, чем все остальные антигипертензивные средства, уменьшают МАУ и ПУ (на 40–50%) и в 5-6 раз замедляют темпы снижения СКФ (рис. 5). Их своевременное назначение позволяет на 25–30 лет отсрочить развитие тХПН и потребность в заместительной почечной терапии. Кроме того, иАПФ и БРА эффективно предупреждают часто сопутствующую ДН сердечно-сосудистую патологию – развитие инсульта и острого инфаркта миокарда, превосходят другие препараты по способности снижать выраженность гипертрофии миокарда, являются препаратами выбора для лечения сопутствующей недостаточности кровообращения. В качестве перспективных средств нефропротекции и контроля АД при ДН могут также рассматриваться прямые блокаторы ренина. Препараты гликозоаминогликанов – веществ, входящих в состав базальной мембраны почек, которые обеспечивают избирательную проницаемость почечного фильтра для белков, в комбинации с основной патогенетической терапией иАПФ или БРА доказали высокую эффективность в уменьшении уровня экскреции альбумина на ранней стадии ДН.
При снижении СКФ менее 15 мл/мин показан перевод на заместительную почечную терапию – гемодиализ или перитонеальный диализ. Радикальным методом лечения этой стадии ДН является трансплантация почки, которая позволяет полностью социально реабилитировать больного.
Показатели 3-летней выживаемости пациентов с СД на гемодиализе – 32%, на перитонеальном диализе – 34%, что практически в 2 раза ниже, чем после трансплантации почки, которая признана методом выбора лечения у пациентов с СД.
Девятилетний опыт наблюдения больных СД с тХПН в отделении гемодиализа ФГУ ЭНЦ с использованием мультидисциплинарного подхода в лечении при совместном наблюдении эндокринолога и нефролога с привлечением специалистов по диабетической стопе, кардиологов и офтальмологов позволяет радикально улучшить прогноз выживаемости и качество жизни этой категории больных и провести адекватную подготовку к трансплантации почки.
СИНДРОМ ДИАБЕТИЧЕСКОЙ СТОПЫ
Синдром диабетической стопы (СДС) объединяет ряд поражений стоп с высоким риском ампутаций нижних конечностей, что ведет к ранней инвалидизации и огромным экономическим затратам на лечение и медико-социальную реабилитацию.
У больных СД ампутации проводятся в 17–45 раз чаще, чем в общей популяции. Согласно данным Государственного регистра, частота ампутаций у больных СД в России варьирует от 0,76 до 18,2 случаев на 1000 пациентов, из них от 48,9 до 60% составляют большие ампутации, при которых послеоперационная летальность достигает 50%. В большинстве случаев ампутации предшествуют длительно незаживающие язвы стоп.
Ежегодная частота новых случаев образования язвенных дефектов стоп у больных СД составляет от 1 до 4%, а распространенность данной формы СДС – 4–10%.
Все это определяет чрезвычайную актуальность проблемы ранней диагностики поражений нижних конечностей и диктует необходимость организации системы специализированной помощи и длительного наблюдения за больными группы высокого риска.
Важнейшим условием организации эффективной помощи больным с CДC является мультидисциплинарный подход с организацией работы специализированных кабинетов и отделений «Диабетическая стопа». Именно кабинеты «Диабетическая стопа» в качестве первичного звена должны заменить систему первичной хирургической помощи на базе поликлиник, не соответствующую современным требованиям.
За годы реализации программы «Сахарный диабет» в России создано более 100 кабинетов «Диабетическая стопа» в 50 регионах РФ.
Частота сопутствующих хронических осложнений СД у больных с СДС составляет 90%, причем более чем в 70% случаев пациенты нуждаются в специализированном лечении (ЛФК, витрэктомии, заместительной почечной терапии гемодиализом и т.д.). В связи с этим второе звено специализированной комплексной помощи больным с поражениями нижних конечностей должно быть представлено специализированными отделениями на базе центров, обладающих возможностями мультидисциплинарной диагностической и лечебной помощи.
По мировому опыту известно, данная модель организации системы специализированной помощи больным с СДС позволяет снизить частоту высоких ампутаций на 62% (с 7,4 до 2,8 на 100 тыс. человек в общей популяции), а также общей частоты ампутаций на 40,3%. В расчете на каждые 10 000 человек с СД было отмечено снижение общей частоты ампутаций на 70% (с 53,2 до 16,0), частоты высоких ампутаций на 82% (с 36,4 до 6,7).
Наряду со стандартными методами выявления СДС: осмотр ног, который должен проводиться при каждом посещении врача; оценка неврологического статуса (исследование вибрационной чувствительности, определение болевой, тактильной и температурной чувствительности, определение сухожильных рефлексов, электромиография); оценка состояния артериального кровотока (ультразвуковая допплерография); рентгенография стоп и голеностопных суставов, должны более широко внедряться высокотехнологичные методы диагностики: дуплексное сканирование артерий нижних конечностей, транскутанная оксиметрия, КТ или МРТ ангиография, рентгеновская ангиография, КТ или МРТ стоп, компьютерная педобарография.
Одним из ключевых компонентов лечения пациентов с CДС является иммобилизация пораженной конечности. До появления современных иммобилизирующих приспособлений использовались костыли, кресло-каталка и постельный режим. В отделении диабетической стопы ФГУ ЭНЦ впервые в России стала широко использоваться технология индивидуальных разгрузочных повязок (ИРП) – Total contact cast (ТСС) из современных полимерных материалов, которая позволяет в 2,5-3 раза сократить сроки заживления трофических язв стопы.
Среди комплексных мер по ведению больных с хроническими язвами обработка раны является абсолютно необходимой составляющей лечебной тактики. Гидрохирургическая система «VersaJet» является новейшим методом, предназначенным для удаления некротических тканей. В основе системы – использование водоструйных технологий в высоком скоростном режиме. Безусловным преимуществом гидрохирургического метода обработки ран является малая травматизация здоровых тканей. Использование гидрохирургической системы «VersaJet» сокращает сроки заживления и потребность в хирургических вмешательствах.
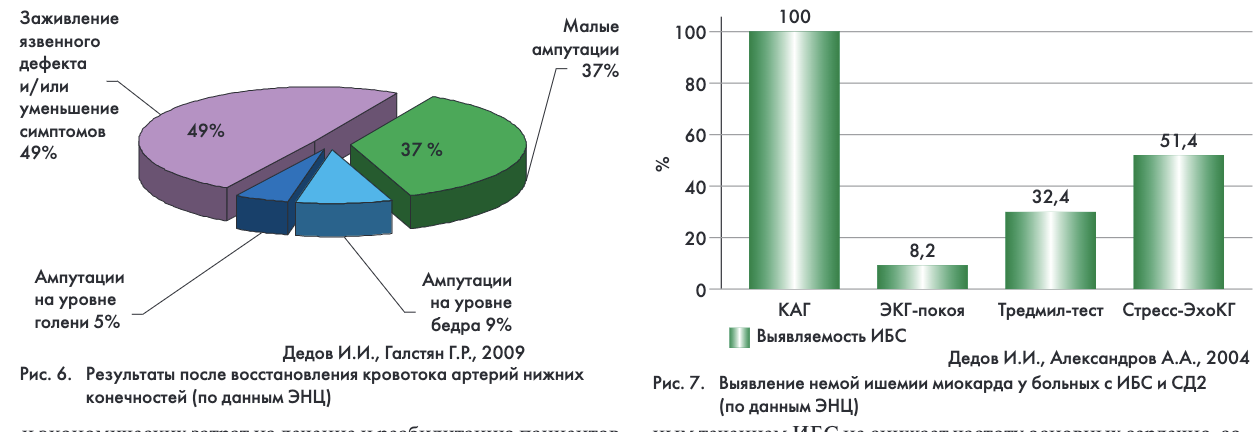
Ишемия конечности вследствие окклюзирующего поражения артерий является одной из основных причин замедления или отсутствия заживления язв у больных СД. На сегодняшний день ангиопластика является наиболее эффективным методом восстановления кровотока. Различные виды оперативного лечения (эндартерэктомия, баллонная ангиопластика, стентирование, дистальное шунтирование) применимы в 90% случаев ишемии нижних конечностей. Своевременное ангиохирургическое вмешательство позволяет сократить сроки заживления, предупредить рецидивирование язвы, избежать выполнения ампутации и сохранить опорную функцию стопы у 86% пациентов с СД (рис. 6).
В большинстве случаев развитие хронических язв нижних конечностей можно предупредить. Особое значение для профилактики СДС имеет достижение стабильного гликемического контроля, коррекция гипертонии и дислипидемии. Простые профилактические приемы: уход за ногами, ежедневный осмотр стоп, ношение ортопедической обуви и регулярное наблюдение в кабинете диабетической стопы не реже 3-4 раз в год, а у пациентов высокого риска ежемесячно – позволяют предупредить образование язвенных дефектов. Обеспечение мер профилактики в комплексе с оптимальной организацией лечебно-диагностического процесса является наиболее эффективным методом снижения риска ампутаций, уровня инвалидизации и экономических затрат на лечение и реабилитацию пациентов с СДС.
СЕРДЕЧНО-СОСУДИСТЫЕ ОСЛОЖНЕНИЯ
СД является мощным фактором развития и прогрессирования сердечно-сосудистой патологии. Развитие СД повышает риск сердечно-сосудистой смертности в 2 раза у мужчин и в 4 раза у женщин, что определяет этих пациентов в категорию высокого и очень высокого сердечно-сосудистого риска.
Ишемическая болезнь сердца (ИБС) по-прежнему остается одной из основных причин смертности пациентов с СД. При этом лишь около 50% пациентов СД знают о наличии у них сердечно-сосудистых заболеваний. Частота безболевой формы ИБС при СД достигает 30-50%, до 25% инфарктов миокарда (ИМ) у пациентов СД протекают бессимптомно.
Проблема диагностики ИБС у больных СД заключается в высокой частоте ЭКГ –негативных форм без депрессии сегмента ST.
Заключение
Диабетология является одним из самых динамично развивающихся направлений современной медицины. За последнее десятилетие в мире и, в том числе, в России достигнутбеспрецедентный по своей значимости прогресс в диагностике, лечении и профилактике СД и его осложнений. Внедрены новейшие инсулины и их аналоги, инновационные сахароснижающие препараты, современные средства мониторинга гликемии и непрерывной подкожной инфузии инсулина, высокотехнологичные методы диагностики и лечения диабетической ретинопатии, нефропатии, синдрома диабетической стопы, кардиальной патологии. Наряду с консервативными методами профилактики сосудистых осложнений широко внедряются интервенционные и эндоваскулярные
технологии восстановления кровотока при поражении коронарных и периферических артерий, что во многих случаях позволяет избежать острых сосудистых катастроф и ампутаций, социально адаптировать и восстанавливать трудоспособность пациентов. В практику диабетологов вошли
иммунологические маркеры и молекулярно-генетические исследования, позволяющие прогнозировать риск развития СД и его осложнений. В обозримом будущем станет возможным проведение полногеномного сиквенса.
Вместе с тем остается множество нерешенных проблем, в первую очередь, организационного характера. Непоправимый урон, который наносит СД и его поздние осложнения здоровью человека и обществу в целом, требует направить максимальные усилия на создание эффективных программ профилактики и активного скрининга с целью ранней диагностики СД и его осложнений. Обеспечение профилактики наряду с мультидисциплинарным подходом в лечении СД является залогом успешного лечения и сохранения качества жизни и здоровья наших пациентов





